1) з'ясувати насамперед, яка саме з вихідних речовин узята у надлишку, бо надлишок не реагуватиме;
2) дальші обчислення робити за тією речовиною, яка прореагувала повністю.
Зверніть увагу, що пвд час розв'язування задач можливі різні варіанти.
Для прикладу розглянемо розв'язування конкретних задач.
Задача 1. До розчину, який містить 1,42 г сульфату натрію, долили розчин, що містить 2,8 г нітрату барію. Утворений осад відфільтрували. Які речовини містяться у фільтраті?
Дано: m (Na2SO4) =1,42 г
Речовини у фільтраті = ?
Аналізуючи умову задачі, бачимо, що для обох солей, які реагують одна з одною, зазначена певна маса, яка може бути стехіометричною. Але, як правило, це ознака того, що задача на надлишок, а він не реагуватиме. Тому визначаємо передусім, яка з вихідних речовин узята у надлишку. Для цього складаємо рівняння реакції:
1,42 г 2,8 г
Na2SO4 + Ba (NO3)2 = BaSo4¯ + 2NaNO3
М = 46+32+64 = М =137+28+96 =
= 142 г/моль = 261 г/моль
m = 142 г m = 261 г
З рівняння реакції видно, що 142 г Na2SO4 взаємодіє із 261 г Ва(NO3)2, а якщо Nа2SO4 узято 1,42 г, тобто у 100 раз менше, то й маса Ва(NO3)2, що реагуватиме, буде у 100 раз меншою —2,61 г. Отже, нітрат барію Ва(NO3)2 узято у надлишку. Цей надлишок становитиме: 2,8 г - 2,61 г = 0,19 г, і міститиметься він у фільтраті разом з нітратом натрію NaNO3, який залишився в розчині, коли осад ВаSO4 відфільтрували.
Відповідь: у фільтраті містяться нітрат натрію NаNОз і надлишок нітрату барію Ва(NO3)2 .
Задача 2. У розчин, що містить їдкий натр масою 20 г, пропустили оксид сульфуру (IV) об'ємом 15 л (н.у.). Визначте масу солі, яка утворилась внаслідок реакції.
Дано: m (NaOH) =20 г
m(солі) = ?
Ознакою того, що дана задача на надлишок, є зазначення в її умові данихобох речовин, що взаємодіють між собою. Тож потрібно спочатку з'ясувати, яка речовина узята у надлишку. Для цього слід скласти рівняння реакції. Але як це зробити, якщо ми не знаємо, яка сіль утворилась? Адже може бути або середня, або кисла сіль. Якщо надлишок їдкого натру, то утворюється середня сіль, а якщо надлишок оксиду сульфуру (ІV), то—кисла сіль (чому? Обґрунтуйте).
Припускаємо, що утворилася середня сіль, тоді .
Перший спосіб
1)Яка з вихідних речовин у надлишку, якщо утворюється середня сіль?
2NaOH + SO2 = Na2So4 + H2O
v = 2 моль v = 1 моль
M = 40 г/моль Vm = 22,4 л/моль
m = 40 × 2 = 80 г V = 22,4 л
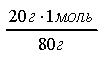 Дізнаємось, яку кількість речовини становлять 20 г NаОН:
Дізнаємось, яку кількість речовини становлять 20 г NаОН:
V(NaOH) = = 0,25 моль
З'ясовуємо мольне співвідношення речовин, які взаємодіють. З рівняння реакції видно, що
v(NaOH): v(SO2)= 2:1,
тобто кількість речовини SO2 вдвічі менша, отже, якщо взаємодіє 0,25 моль NаОН, то SO2 — вдвічі менше, а саме 0,125 моль:
2:1 = 0,25:0,125.
Обчислюємо, яку кількість речовини становлять 15 л SO2:
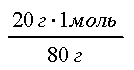
V(NaOH) = = 0,25 моль
0,67 > 0,125, отже, SO2 у надлишку.
А ми вже знаємо, якщо SO2 у надлишку, то утворюється кисла сіль (чому?). Складаємо інше рівняння реакції і за ним перевіряємо, чи справді сіль кисла, й обчислюємо її масу:
NaOH + SO2 = Na2SO4
_ _
v = 1 моль v = 1 моль M = 104 г/моль
M = 40 г/моль Vm = 22,4 л/моль m = 104 г
m = 40 г V = 22,4 л
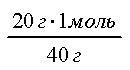
V(NaOH) = = 0,5 моль
v(NaOH) : v(SO2) = 1 : 1; 1 : 1 = 0,5 : 0,5;
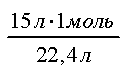
v(SO2) = = 0,67 моль
0,67>0,5, отже, SO2 у надлишку, сіль—кисла.
Це означає, що подальші розрахунки треба проводити за Їдким натром, оскільки він прореагував повністю.
2) Яка маса утвореної солі?
m=M · v
m(NаНSO3) =104 г/моль · 0,5 моль = 52 г.
Відповідь: m(NаНSO3) = 52 г.
Другий спосіб
1) Яка з вихідних речовин у надлишку, якщо утворюється середня сіль?
20г 15л
2NaOH + SO2 = Na2SO4 + H2O
_
v = 2 моль v = 1 моль
M = 40 г/моль Vm = 22,4 л/моль
m = 80 г V = 22,4 л
З рівняння реакції видно, що 80 г NаОН повністю взаємодіють з 22,4 л SO2, а 20 г NаОН —з х л SO2,
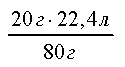 отже:
отже:
80 : 20 = 22,4: х;x = =5,6 л(SO2)
За умовою задачі пропускали 15 л SO2, а прореагувало лише 5,6 л. Отже, оксид сульфуру (ІV) взято у надлишку. Це означає, що сіль, яка утворюється, кисла. У такому разі треба скласти інше хімічне рівняння і за ним перевірити, чи справді утворюється кисла сіль:
NaOH + SO2 = NaHSO3
_ _
v = 1 моль v = 1 моль M = 104 г/моль
M = 40 г/моль Vm = 22,4 л/моль m = 104г
m = 40 г V = 22,4 л
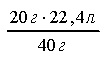
40 : 20 = 22,4 : х; х = = 11,2 (SO2)
Сіль кисла NаНSO3, і у даному разі SO2 у надлишку.
2) Тепер можна обчислювати масу утвореної солі. Ви пам'ятаєте, що розрахунок ведеться за речовиною, яка прореагувала повністю, тобто за гідроксидом натрію NаОН.
З рівняння реакції видно, якщо взаємодіє SO2 i 40 г NаОН, то утворюється 104г NаНSO3, а якщо з SO2 взаємодіє 20 г NаОН, то —х г солі гідросульфіту натрію:
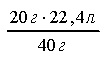
40 : 20 = 104 : х; x = = 52 г.
Відповідь: m(NаНSO3) = 52 г.
6. СУЛЬФАТНА КИСЛОТА
Сульфатна кислота H2SO4 (безводна, 100 %-ва) —важка безбарвна оліїста рідина. Густина її концентрованого розчину (w(H2SO4) == 98 %) за звичайних умов 1,84 г/см3. Вона нелетка, запаху не має. Надзвичайно гігроскопічна. Активно вбирає вологу. Змішується з водою у будь-яких співвідношеннях. Розчинення сульфатної кислоти у воді супроводжується виділенням великої кількості теплоти, що може призвести до закипання води і розбризкування кислоти.
Сульфатна кислота—їдка рідина, тому треба остерігатись, щоб вона не потрапила на шкіру й одяг. А якщо це сталося, треба швидко змити її великою кількістю води, після чого нейтралізувати розчином соди і знову змити водою.
Пам'ятайте таке правило:
не можна воду доливати до концентрованої сульфатної кислоти! Для розбавляння кислоту треба доливати до води невеликими порціями.
Хімічні властивості сульфатної кислоти багато в чому залежать від її концентрації. В лабораторіях та промисловості використовують розбавлену і концентровану сульфатну кислоту, хоча такий поділ дещо умовний.
