h - постійна Планка (h=6,626*10-34 Дж*с).
В 1905 р. Альберт Ейнштейн доказав, що будь-яке випромінення складається з дискретних частинок - квантів випромінення, які називаються фотонами. В результаті цих досліджень виникло уявлення про подвійну природу світла. А в 1924 р. Луі де Бройль розповсюдив це уявлення на електрони і пояснив корпускулярно-хвильовий дуалізм поведінки електрона.
Сучасна квантова механіка базується на планетарній моделі Бора, а також на принципі заборони Паулі. (Докладно розглядається далі). Цей принцип точно визначив розташування електронів на дискретних енергетичних рівнях навколо ядра. В 1926 р. Ервін Шредінгер запропонував математичне рівняння для опису руху субатомних частинок. Кульмінацією розвитку квантової механіки є дослідження Поля Дірака, який зміг теоретично пояснити корпускулярно-хвильовий дуалізм елементарних частинок.
Розглянуті вище дослідження дозволили сформулювати ряд положень, що складають сучасні уявлення науки про будову атома :
2.2. Електронна Будова Атома
Обґрунтувати теорію електронної будови дозволяють сучасні методи дослідження атомних спектрів та енергій іонізації атомів. Будь-який спектр є розкладом випромінення на компоненти. Відповідно до моделі Бора електрони в атомах обертаються навколо ядра по кругових орбітах, чи оболонках. Кожна оболонка має строго визначений енергетичний рівень і характеризується деяким квантовим числом N. Чим більше N , тим вище енергетичний рівень оболонки. Оболонки одержали літерне позначення K, L, M, N і далі в порядку латинського алфавіту, кожній оболонці відповідає своє квантове число N. Для K оболонки N = 1, для L - N = 2, для M - N=3 і т.д. На кожній оболонці може знаходитися не більше визначеного числа електронів, і їхнє максимальне число індивідуальне для кожної оболонки.
|
Оболонка |
квантове число N |
макс. число електронів |
|
K |
1 |
2 |
|
L |
2 |
8 |
|
M |
3 |
18 |
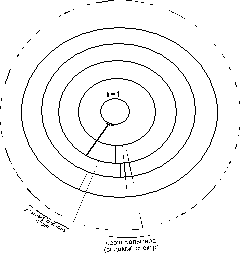 Перехід електрона з однієї оболонки на іншу можливий при поглинанні чи випусканні кванта електромагнітного випромінювання з енергією, що дорівнює різниці енергій рівнів, між якими пересувається електрон. Тому оптичні спектри поглинання атомів, що відповідають електронним переходам на дискретні вільні рівні, так само повинні бути дискретні.
Перехід електрона з однієї оболонки на іншу можливий при поглинанні чи випусканні кванта електромагнітного випромінювання з енергією, що дорівнює різниці енергій рівнів, між якими пересувається електрон. Тому оптичні спектри поглинання атомів, що відповідають електронним переходам на дискретні вільні рівні, так само повинні бути дискретні.
Модель Бора не могла пояснити особливості спектрів елементів більш складних ніж водень. Крім того, електрон розглядалася як частка, що приводило до ряду протиріч. Більш пізні дослідження показали, що електрон має хвильову природу і йому варто приписати визначену довжину хвилі, що залежить від його енергії. Це положення, висунуте Луї де Бройлем, лягло в основу квантової механіки, методи якої в даний час використовуються для розрахунку властивостей атомів, молекул і твердих тіл, що з них складаються.
2.3.Орбіталі.
 | 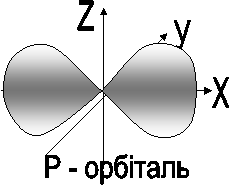 | ||
Орбіталі часто називають підоболонками оболонок, оскільки вони характеризують форми різних орбіт, на яких можна знайти електрони, що знаходяться в одній оболонці (при заданому квантовому числі N). Кожна підоболонка характеризується своїм, побічним квантовим числом L (його називають орбітальним) . Воно, так само як і Nа, ціле і може змінюватися в межах від 0 до (N-1). Орбітали однієї підоболонки в звичайних умовах мають однакові значення енергії (вирождені), однак під впливом зовнішнього магнітного поля орбітальні енергії стають дискретними чи квантованими.
Магнітне квантове число M цих дискретних енергетичних рівнів може приймати цілочисленне значення в межах від -L до L (включно), тобто воно може приймати 2L+1 значень. Четверте квантове число S (спін) характеризує обертання окремого електрона і може приймати значення: +1/2 і -1/2.
Кожен електрон в атомі повинний мати свій індивідуальний набір квантових чисел. Знаючи головне квантове число N, легко розрахувати, скільки електронів може знаходитися на тій чи іншій оболонці й оцінити форму можливих орбіталей.
При утворенні молекул і кристалів з атомів, на зовнішній (валентній) оболонці яких маються як S так і P електрони, можливе змішування (інтерференція) їхній орбіталей і утворення "гібридних" SP орбіталей. Форма гібридної орбіталі залежить від того, скільки P орбіталей бере участь у її утворенні. Приклади можливих гібридних орбіталей показані на нижньому малюнку.
Структура молекул і кристалів буде залежати від того, які орбітали беруть участь в утворенні хімічного зв'язку між атомами. В утворенні таких напівпровідникових кристалів як Si і Ge беруть участь SP3 -орбіталі (приналежні різним оболонкам).
При цьому, у результаті взаємодії атомів, дискретні рівні можуть бути розглянуті як енергетичні зони. У напівпровідниках із двох сусідніх зон, що утворилися з рівнів валентних електронів, одна виявляється заповненою, друга вільною.
2.4.Склад атомних ядер.
Масове число (А)- це сумарне число протонів і нейтронів в ядрі атома. Атомний номер (Z)елемента співпадає з числом протонів в ядрі його атома.
A=Z+N, де N-число нейтронів в ядрі атома. Кожен хімічний елемент характеризується певним атомним номером. Тобто два елемента не можуть мати однаковий атомний номер.
Ізотопами - називають різні за властивостями атомні різновиди одного елемента. Вони розрізняються по кількості нейтронів в їх ядрі. Таким чином, ізотопи одного елемента мають однаковий атомний номер, але різні масові числа. Наприклад,
612С, 613 С, 614 С – ізотопи вуглецю.
Атомна одиниця маси ( а.о.м.).
За стандарт прийнята маса стабільного ізотопу вуглецю
612С = 12,0000а.о.м., таким чином 1 а.о.м. =1/12m612С.
Істине значення а.о.м.= 1,661*10-27кг.
